 设为首页
设为首页
 加入收藏
加入收藏
扩展资料
等温变化玻意耳定律
1、玻意耳定律
一定质量的气体,在温度保持不变时,它的压强和体积成反比;或者说,压强和体积的乘积保持不变.它的数学表达式为:
![]() 或
或 ![]() 或
或 ![]() (常数)
(常数)
2、玻意耳定律的适用条件
(1)温度不太低,压强不太大
(2)被研究气体的质量、温度保持不变

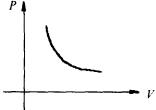
3、气体的等温变化(如左上图所示)
(1)图线上每一点表示气体处于某一特定的状态
(2)图线上各点连起来的曲线表示气体的变化过程
(3)当以P为纵坐标,
![]() 为横坐标,图线形状变为如右上图所示的形式
为横坐标,图线形状变为如右上图所示的形式
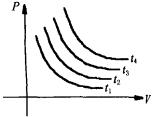
(4)玻意耳定律表示一定温度下,气体的压强和它的体积的关系,由此可知此定律表达式中的恒量跟温度有关系.实验表明:温度越高,恒量C越大,等温线离坐标轴越远.如图所示4条等温线的关系为
![]()
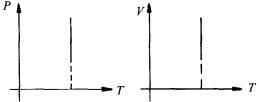
(5)在
![]() 坐标,
坐标, ![]() 坐标中表示等温线如图所示.
坐标中表示等温线如图所示.
4、应用玻意耳定律解题的一般步骤
(1)明确研究对象是哪一部分气体;
(2)确定初、末状态及其状态参量(
![]() );
);
(3)由
![]() 列式求解,必要时考虑结果是否合理.
列式求解,必要时考虑结果是否合理.
扩展资料
查理定律的图像表示――等容图线.
(1)
![]() 图中的等容线
图中的等容线
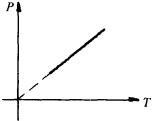
①如图所示,图线是一条不过原点的直线,图线与横轴的交点是-273℃,与纵轴的截距等于该气体在℃时的压强.

②图线的斜率 ![]() ,
, ![]() 与气体的种类、质量和体积均有关.
与气体的种类、质量和体积均有关.
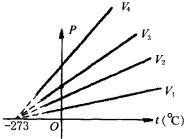
③对于一定质量的同种气体,等容线的斜率和气体保持不变的体积大小有关.体积越大,斜率越小.如图所示四条等容线的体积关系为:
![]()
(2)
![]() 图中的等容线
图中的等容线
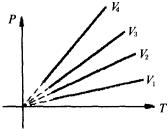
①如图所示,是一条延长线过原点的直线
②斜率
![]() ,与
,与 ![]() 图线中的斜率相同.∴体积越大,斜率越小.如图所示为四条等容线所表示的体积关系:
图线中的斜率相同.∴体积越大,斜率越小.如图所示为四条等容线所表示的体积关系:
![]()
扩展资料
盖・吕萨克定律知识讲解
由 ![]() 可知;当P一定时,
可知;当P一定时, ![]() (恒量).此关系最初是法国科学家盖・吕萨克研究气体膨胀时得到的实验定律.
(恒量).此关系最初是法国科学家盖・吕萨克研究气体膨胀时得到的实验定律.
盖・吕萨克定律的表述如下:
(1)第一种表述:一定质量的气体,在压强保持不变时,体积和
热力学温度成正比,其表达式为:
![]() 或
或 ![]() (恒量)
(恒量)
式中
![]() 的大小与该定质量气体的压强有关,气体压强越大C值越小.
的大小与该定质量气体的压强有关,气体压强越大C值越小.
(2)第二种表述:一定质量的气体,在保持压强不变的情况下,温度每升高(或降低)1℃,增加(或减小)的体积等于它在0℃时体积的
![]() ,其表达式为
,其表达式为
![]() 或
或 ![]()
(3)此定律的适用条件:适用于一切理想气体,即,温度不太低,压强不太大的气体.
(4)V-T和V-t图中的等压线表示分别如图所示.
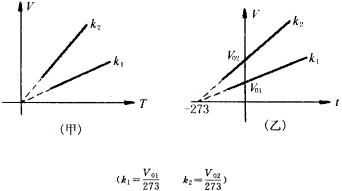
![]() ――是该定质量气体在0℃时的体积.
――是该定质量气体在0℃时的体积.
斜率k数值上等于 ![]() .其大小取决于气体保持不变的压强的大小,压强越大,k越小,如图,
.其大小取决于气体保持不变的压强的大小,压强越大,k越小,如图,
![]()
扩展资料
“吊针瓶”的药液为何匀速满注?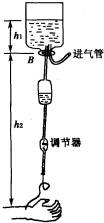
一般人认为是因为“吊针”上的调节器控制的结果,这是错误的,调节器作用类似水池底部有一水龙头,而随着水位下降,水龙头中水流速度减慢,水龙头是不能控制水的匀速流出的.
真正的原因是:如图所示,随着瓶内药液面的降低,瓶内液面上气体压强变小,外界空气在大气压作用下通过过气管不断进入瓶内上部,总保持瓶内气体压强与 ![]() 段液柱产生的压强和等于大气压,所以在针头处药液的压强为
段液柱产生的压强和等于大气压,所以在针头处药液的压强为 ![]() ,因
,因 ![]() 不变,所以药液压强
不变,所以药液压强 ![]() 保持恒定,而病人的血压在短时间内一般不变,从而使注射压
保持恒定,而病人的血压在短时间内一般不变,从而使注射压 ![]() 相对稳定,从而保证“吊针”在整个输液过程中能始终匀速滴注.关键是由于进气管的存在使瓶口处药液的压强始终保持为大气压不变.
相对稳定,从而保证“吊针”在整个输液过程中能始终匀速滴注.关键是由于进气管的存在使瓶口处药液的压强始终保持为大气压不变.