 设为首页
设为首页
 加入收藏
加入收藏
重点:溶解度的概念,固体溶解度曲线的含义与应用
难点:溶解度的概念,固体溶解度曲线的含义与应用
教学过程:
[引言]通过前面的学习我们已经知道,酒精可以任意比例与水互溶,那么,在一定温度下,一定量的溶剂所能溶解的溶质的质量有没有一个限度呢?我们用什么方法来表示这种限度呢?
[板书]第三节 溶解度
[思考]
从日常生活中寻找实例,说明气体在水中溶解性受哪些外界条件的影响,这些条件对气体的溶解性产生怎样的影响。
[板书]一、溶解度
[讲解]溶解性是物质的一个重要性质,怎样才能比较精确地表示一种物质在水中溶解性的大小呢?
[板书]1.固体物质的溶解度
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
[布置思考题]理解溶解度概念时应注意哪些问题?
[板书]关键词:一定温度(指条件);100g溶剂;饱和溶液;克(单位)。
[布置讨论题]“20℃时食盐溶解度是36g”的含义是什么?
[板书]2.溶解度曲线
[讲解]在平面直角坐标系中溶解度的大小与温度有关。可以以横坐标表示温度,以纵坐标表示溶解度,画出物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
[板书]溶解度随温度变化的曲线叫做溶解度曲线。
[展示教学挂图]
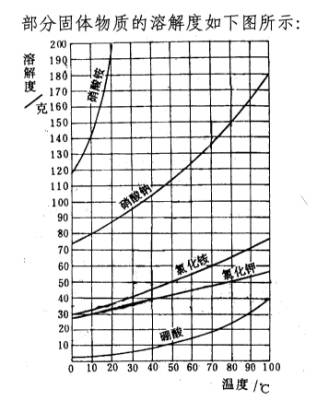
[布置学生讨论]从溶解度曲线中我们可以获取什么信息?
[师生共同归纳]
1.溶解度曲线从溶解度曲线中可以查到有关物质在一定温度下的溶解度;可以比较相同温度下不同物质的溶解度以及各物质溶解度随温度变化的趋势等等。
2.从溶解度曲线可以看出,大多数固体物质的溶解度随温度的升高而增大,如硝酸铵、硝酸钾等;有些与温度的变化关系不大,如氯化钠。利用溶解度曲线提供的信息,可以对某些物质组成的混合物进行分离。
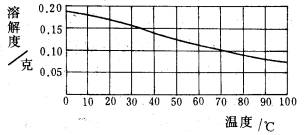
[讲解]对大多数物质来说,其溶解度都是随温度的升高而增大的,也有些固体物质,其溶解度是随着温度的升高而减小,氢氧化钙就是这样一种物质。
[展示教学挂图]氢氧化钙溶解度曲线
[板书]气体的溶解度:通常用“1体积水中所能溶解气体的体积”来表示气体的溶解度。
气体的溶解度随温度的升高而减小,随压强的升高而增大。
[展示表格]
|
[板书]二、混合物的分离
[布置讨论题]把食盐和硝酸钾放入水中,他们会逐渐溶解形成溶液。用什么方法可以把他们从溶液中分离出来?
[学生分组实验]
[板书]1.蒸发食盐水:
(在蒸发皿中注入少量饱和食盐水加热蒸发,用玻璃棒不断搅拌,冷却后有晶体析出。利用蒸发溶剂的方法适用于该物质的溶解度岁温度升高变化不大,可以得到该物质的晶体。)
设计思想:
溶解度是第七章教学的重点和难点。传统教学模式把溶解度概念强加给学生,学生对概念的理解并不深刻。本节课从比较两种盐的溶解性大小入手,引发并活跃学生思维,设计出合理方案,使其主动地发现制约溶解度的三个条件,然后在教师引导下展开讨论,加深对"条件"的认识。这样设计,使以往学生被动的接受转化为主动的探索,充分调动了学生善于发现问题,勇于解决问题的积极性,体现了尝试教学的基本观点:学生在教师指导下尝试,并尝试成功。
教学目标:
1、理解溶解度概念。
2、了解温度对溶解度的影响。
3、了解溶解度曲线的意义。
教学器材:胶片、幻灯机。
教学方法:尝试教学法 教学过程:
一、 复习引入
问:不同物质在水中溶解能力是否相同?举例说明。
答:不同。例如食盐能溶于水,而沙子却极难溶于水。
问:那么,同种物质在不同溶剂中溶解能力是否相同?
答:不同。例如油易溶于汽油而难溶于水。
教师总结:
物质溶解能力不仅与溶质有关,也与溶剂性质有关。通常我们将 一种物质在另一种物质中的溶解能力叫溶解性。
二、讲授新课
1、 理解固体溶解度的概念。
问:如何比较氯化钠、硝酸钾的溶解性大小?
生:分组讨论5分钟左右,拿出实验方案。
(说明:放给学生充足的讨论时间,并鼓励他们畅所欲言,相互纠错与补充, 教师再给予适时的提示与总结。学生或许会凭感性拿出较完整的实验方案,意识到要比较氯化钠、硝酸钾溶解性大小,即比较在等量水中溶解的氯化钠、硝酸钾的多少。但此时大多数学生对水温相同,溶液达到饱和状态这两个前提条件认识不深刻,教师可引导进入下一次尝试活动。)
问:
(1)为什么要求水温相同?用一杯冷水和一杯热水分别溶解氯化钠和硝酸钾,行不行?
(2)为什么要求水的体积相同?用一杯水和一盆水分别溶解,行不行?
(3)为什么要达到饱和状态?100克水能溶解1克氯化钠也能溶解1克硝酸钾,能否说明氯化钠、硝酸钾的溶解性相同? 生:对上述问题展开积极讨论并发言,更深入的理解三个前提条件。
(说明:一系列讨论题的设置,充分调动了学生思维,在热烈的讨论和积极思考中,"定温,溶剂量一定,达到饱和状?这三个比较物质溶解性大小的前提条件,在他们脑海中留下根深蒂固的印象,比强行灌输效果好得多。)
师:利用胶片展示完整方案。
结论:1、10℃时,氯化钠比硝酸钾更易溶于水。
师:若把溶剂的量规定为100克,则某温度下100克溶剂中最多溶解的溶 质的质量叫做这种溶质在这个温度下的溶解度。
生:理解溶解度的涵义,并思考从上述实验中还可得到什么结论?
结论:2、10℃时,氯化钠的溶解度是35克,硝酸钾的溶解度是21克。
生:归纳溶解度定义,并理解其涵义。
2、根据溶解度判断物质溶解性。
师:在不同的温度下,物质溶解度不同。这样,我们只需比较特定温度下 物质溶解度大。生:自学课本第135页第二段并总结。
3、溶解度曲线。
师:用胶片展示固体溶解度曲线。
生:观察溶解度曲线,找出10℃时硝酸钠的溶解度及在哪个温度下,硝酸钾 溶解度为110克。
问:影响固体溶解度的主要因素是什么?表现在哪些方面?
答:温度。大多数固体溶解度随温度升高而增大,例如硝酸钠;少数固体 溶解度受温度影响不大,例如氯化钠;极少数固体随温度升高溶解度反而减小,例如氢氧化钙。
板书:
一、固体溶解度
1、定义:
①定温 ②100克溶剂 ③饱和状态 实质:溶解溶质质量。
2、难溶 微溶 可溶 易溶
0.01 1 10 S (20℃)
3、固体溶解度曲线。
二、课堂巩固练习
1、下列关于溶解度说法正确的是( )
A、一定温度下,该物质在100克溶剂中所溶解的克数。
B、一定温度下,该物质在100克饱和溶液中所含溶质的克数。
C、该物质在100克溶剂中达到饱和状态所溶解的克数。
D、一定温度下,该物质在100克溶剂中最多能溶解的克数。
2、已知60℃时,硝酸钾的溶解度是110克。
(1)指出其表示的含义。
(2)在60℃硝酸钾饱和溶液中,溶质、溶剂、溶液质量比为?
(3)向100克水中加入80克硝酸钾,溶液是否饱和?加入120克呢?
3、已知20℃时,100克水中最多能溶解20.1克某物质,该物质属( )
A、易溶 B、难溶 C、微溶 D、可溶
4、已知20℃时,25克水中最多能溶解0.8克某物质,则该物质属( )
A、易溶 B、微溶 C、可溶 D、易溶
三、复习小结
师:如何认识溶解度?怎样由溶解度判断溶解性大小?
生:回顾本节课知识,进一步加深对上述问题的认识。
四、 布置作业