 设为首页
设为首页
 加入收藏
加入收藏
教学设计方案(一)
第三节 乙烯 烯烃
教学重点:乙烯的分子结构和化学性质,乙烯的实验室制法
教学难点:乙烯的分子结构
教学手段:充分利用多媒体课件,掌握乙烯的分子结构及结构与性质的关系,并通过实验验证结论,突破重点、难点;组织学生自己完成乙烯的实验室制备并对实验进行探究、改进,培养学生的实验能力,强化重点知识。
设计思路:由乙烷作对比,由学生探究出乙烯的分子结构,由结构研究其性质,使学生体会到研究有机化学的方法,由学生动手设计改进实验,提高其思维品质,配合课件,把微观变化宏观化,达到激发兴趣、强化印象、加深理解的目的。
教学过程:
第一课时
[播放录像引入] 录像内容为:一个人正向青香蕉上喷洒一种液体(乙烯利)
[提问] 他要干什么?
[学生讨论发言]
[播放录像] 内容:原来的那堆青香蕉现在变成了黄色。
[指出] 他喷洒的这种液体会释放出一种气体,这种气体对香蕉具有催熟作用,这种气体是什么呢?――乙烯。
[板书] 第三节 乙烯 烯烃
[指出] 乙烯的分子式是 ![]()
[学生练习] 写出乙烷的分子式、电子式、结构式、结构简式
[设问] 对比乙烯和乙烷的分子式思考,乙烯的结构式应如何写?
(提示:有机物中碳原子均满足四价)
[学生讨论、书写]
[教师总结并板书]
一、乙烯的结构
分子式: ![]()
![]()

结构简式: ![]()
[强调] 乙烯分子里出现了C=C双键,它所结合的氢原子个数比乙烷少了两个,像这样碳原子所结合的氢原子数少于饱和链烃里的氢原子数的烃,就叫做不饱和烃。乙烯中的C=C可以看成有一个键相当于乙烷中的碳碳键,另一个碳碳键相当于乙烷去氢之后形成的。
[课件演示] 乙烯的球棍模型和比例模型
[引导学生过观察] 乙烯是平面型结构,键角都是
![]() ,乙烯的C=C中两个键是不一样的,一个稳定,一个不稳定。
,乙烯的C=C中两个键是不一样的,一个稳定,一个不稳定。
[指出] 乙烯不同与乙烷的结构决定了乙烯有不同于烷的化学性质,主要发生在那个易断裂的键上。
[板书] 二、化学性质
[演示实验5-6] 可由学生上台演示。
[分析讲解] 乙烯遇到溴后,发生了下列变化

这种有机物分子中双键(或叁键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
[课件演示] 乙烯与 ![]() 的加成的微观变化
的加成的微观变化
[设问] 哪些物质能和乙烯发生加成反应呢?
[课件演示] 乙烯和 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 的加成
的加成
[电子板书] 1、加成反应


![]()
[过渡] 乙烯和乙烯也能发生加成反应
[课件演示] 乙烯的聚合反应
[指出] 乙烯的这种加成反应形成了相对分子质量很大的物质,我们把这种相对分子质量很大的物质叫作高分子化合物,而像乙烯这样由相对分子质量小的化合物分子互相结合成相对分子质量很大的高分子化合物的反应就叫做聚合反应,乙烯的聚合实质上也是一种加成,因此这种反应也叫做加成聚合反应,简称加聚反应。
[板书] (二)、加聚反应

[学生演示实验5-5] 联想对比与乙烷通入酸性高锰酸钾溶液中现象不同的原因
[讲解] 乙烯能与高锰酸钾反应也是因为有C=C的缘故,此反应与加成反应不同,产物中往往会有 ![]() 生成。
生成。
[板书] (三)、氧化反应
1、 使酸性 ![]() 溶液褪色
溶液褪色
[学生演示5-4] 注意引导观察与乙烷燃烧的不同。
[讨论] 乙烯燃烧为什么会有少量黑烟?
[练习] 写出乙烷燃烧的化学方程式
[板书] 2、燃烧
![]()
[总结] 乙烯属于烃,具有烃的一个通性――燃烧,由于含有C=C,又具有其特性,能被强氧化剂氧化,还能发生加成和加聚反应。
[巩固练习] 可以用哪些方法制备 ![]() ?哪种方法较好?写出有关的反应方程式。
?哪种方法较好?写出有关的反应方程式。
[作业] 完成课本相关内容的习题。
(作者 河北霸州一中 刘彦民)
教学设计方案(二)
第三节 乙烯 烯烃
第二课时
[复习] 微机演示乙烯的球棍模型和比例模型
[提问] 乙烯能发生哪些化学反应?
[指导阅读] 乙烯的用途
阅读提纲:
1、衡量一个国家石油化学工业水平的重要标志是什么?
2、乙烯对果实有催熟作用,它是一种气体,为什么我们在录像中看到喷洒的是一种液体?
[微机展示] 乙烯的用途图片资料,各种以乙烯为原料制出的产品的实物图片。
[过渡] 乙烯如此重要,它是怎么制出来的呢?
[板书] 三、乙烯的制法
(一)、工业制法:从石油中获得
[讲解] 实验室制乙烯的原料和反应原理
[板书] (二)、实验室制法
![]()
[课件演示] 乙醇在浓硫酸作用下变为乙烯的微观变化。
[讨论] 根据反应物和反应条件应选用什么样的装置?(有条件的学校可让学生组装出该装置)
[分组实验] 用排水法收集一瓶乙烯气体(强调温度计的位置、碎瓷片的作用)
(此气体保留,用来研究乙烯的物理性质)
[观察并分组讨论]
1、烧瓶中的液体为什么会变黑?
2、制得的气体为什么会有刺激性气味?
3、如何证明乙烯中混有 ![]() ?
?
4、这种方法制得的乙烯通过溴水时使溴水褪色,能否说明乙烯和溴发生了反应?若不能,应如何改进?
5、为什么要控温170℃?
[分组实验或演示课件] 验证制得的气体中混有
![]() 和改进装置后乙烯使溴水褪色。
和改进装置后乙烯使溴水褪色。
[观察回答] 乙烯的物理性质
[过渡] 在烷烃中我们学习了甲烷、乙烷、丙烷等,那么是否也还有甲烯、丙烯、丁烯等物质呢?
[板书] 四、烯烃
[指导阅读] 请同学们阅读课本相关内容并完成自学提纲:
(一)、什么叫烯烃?
(二)、烯烃的通式是什么?
(三)、通过表5-3中的数据总结烯烃的物理性质有什么变化规律?
(四)、完成下列反应方程式:
![]()
![]()
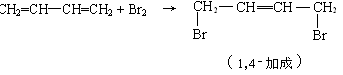
[补充材料] 简介二烯烃及橡胶,重点介绍共轭二烯烃的加成反应(以1,3-丁二烯为例)
[板书]
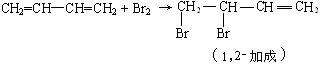

[巩固练习]
1、用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如下图所示,它属于

A.无机物 B.烃 C.高分子化合物 D.有机物
2、关于实验室制乙烯的实验,下列说法正确的是
A.反应物是乙醇和过量的3mol/L的硫酸的混合液
B.温度计插入反应液液面下,以便控制温度在
![]()
C.反应容器(烧瓶)中应加入少许碎瓷片
D.反应完毕后先灭火再从水中取出导管

[作业] 完成课本相关内容的习题
板书设计: 第三节 乙烯 烯烃
一、乙烯的结构
分子式: ![]()
结构式: ![]()
电子式: 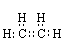
结构简式:CH2=CH2
二、化学性质
(一)、加成反应
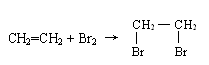
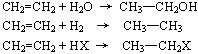
![]()
(二)、加聚反应

(三)、氧化反应
![]()
三、乙烯的制法
(一)、工业制法:从石油中获得
(二)、实验室制法

物理性质:无色、稍有气味的气体,难溶于水,比空气略轻
四、烯烃
(一)、分子里含有碳碳双键的一类链烃叫做烯烃
(二)、通式:CnH2n (n≥2)
(三)、随碳原子个数的增加,烯烃的熔沸点和密度逐渐增大
(四)、化学性质与乙烯类似
![]()
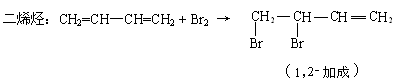
总结:
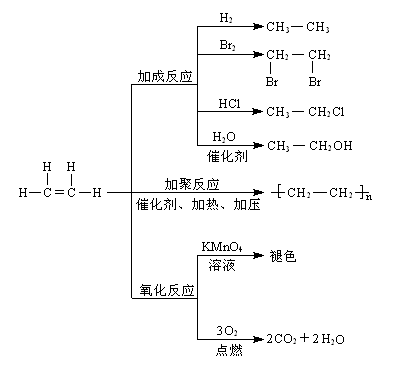
(作者 河北霸州一中 刘彦民)