 设为首页
设为首页
 加入收藏
加入收藏
教材分析
乙炔的化学性质一段内容,在介绍性质之前,教材也是先安排了一个讨论,让学生从分子结构上把乙炔与乙烯、乙烷作一比较,进而推断乙炔可能具有的化学性质。讨论之后,教材又在间接给出讨论思路的同时, 以提问的方式提示寻找讨论题最后答案的途径,这样就使后面的演示实验具有了探索意义,讨论题的最后答案就在一个个实验之后。这样的处理使乙炔性质的介绍既不雷同于乙烯,又通过不饱和键把乙炔同乙烯联系起来,从而突出了官能团的作用。
乙炔的实验室制法教材中没有安排相应的制取实验。而是通过相关的化学方程式告诉学生实验室中使用的乙炔,可以通过电石与水的反应得到。在介绍乙炔化学性质的实验中,安排了这个实验,使学生更加明确物质的制取实验和性质实验之间的关系。
对于炔烃,教材采用的方法与烯烃类似,首先给出炔烃的通式,指出“相邻炔烃之间也是相差一个‘ ![]() ’原子团”。然后,再通过对部分炔烃的主要物理性质的分析,告诉学生炔烃的物理性质与烯烃一样,也随着碳原子数目的增加而发生递变。进而得出由于炔烃中含有碳碳三键,炔烃的主要化学性质与乙炔类似的结论。
’原子团”。然后,再通过对部分炔烃的主要物理性质的分析,告诉学生炔烃的物理性质与烯烃一样,也随着碳原子数目的增加而发生递变。进而得出由于炔烃中含有碳碳三键,炔烃的主要化学性质与乙炔类似的结论。
本节教学重点:乙炔的结构和主要性质。
关于乙炔的实验室制法的教学建议
学生在此之前已经学生过三种制取气体的发生装置,因此有必要讨论制取乙炔的装置。根据反应原理组织学生讨论,能否使用启普发生器?学生在讨论后应明确:
(1) ![]() 不仅能与液态水反应,也能与水蒸气反应,而且反应较剧烈,使用启普发生器难以控制反应速率。
不仅能与液态水反应,也能与水蒸气反应,而且反应较剧烈,使用启普发生器难以控制反应速率。
(2)反应中要放出大量热,启普发生器是厚玻璃壁仪器,容易因胀缩不均,引起破碎。
(3)反应产物 ![]() 微溶于水,易形成糊状泡沫堵塞导气管和球形漏斗的下口。
微溶于水,易形成糊状泡沫堵塞导气管和球形漏斗的下口。
提出为什么实验室制备的乙炔有臭味?(由电石产生的乙炔因常混有 ![]() 、
、 ![]() 等杂质而有特殊难闻的臭味。)
等杂质而有特殊难闻的臭味。)
此外为了减少气态烃不完全燃烧产生的 ![]() 和黑烟对环境的影响,建议组织学生探讨使气态烃充分燃烧的方法。
和黑烟对环境的影响,建议组织学生探讨使气态烃充分燃烧的方法。
乙炔结构和性质的教学建议
由于学生已经有甲烷、乙烯的结构和主要化学性质等知识基础,对有机物的结构和性质的辩证关系也有了一定的理解,并且初步知道了系统地研究饱和烃与不饱和烃的一些方法。建议在教学过程中可进行如下操作。
1.关于乙炔的结构
(1)组织学生复习有关碳原子形成共价键的知识,使学生明确碳原子与碳原子之间不仅能形成单键(C―C)、双键(C=C),而且还能形成三键(C≡C)。
(2)利用球棍模型让学生自己动手,拼出乙炔的结构模型,然后教师进行评价。
(3)通过研究讨论,写出乙炔分子的分子式( ![]() )、乙炔的结构式(H―C≡C―H)、结构简式(HC≡CH)和电子式(H :C
)、乙炔的结构式(H―C≡C―H)、结构简式(HC≡CH)和电子式(H :C ![]() C: H)。明确乙炔分子中含有不饱和碳碳三键。
C: H)。明确乙炔分子中含有不饱和碳碳三键。
(4)明确在乙炔分子中,两个碳原子和两个氢原子处在一条直线上,键是 ![]() 。
。
C≡C叁键的键能是812kJ/mol,比三个C―C单键的键能之和要小得多。
2.根据结构推断乙炔的化学性质
(1)对比乙烯和乙炔的结构,从不饱和烃的性质出发,组织学生探索乙炔可能具有的主要化学性质(可燃性、与 ![]() 酸性溶液反应、与溴反应)。
酸性溶液反应、与溴反应)。
(2)实验验证。注意观察比较乙烯与乙炔的异同。实验前提出观察要求,特别是注意与乙烯进行对比,乙炔与溴水和酸性高锰酸钾溶液反应的速度比乙烯的慢。要求学生分析这一事实说明什么,其实碳碳三键比碳碳双键稳定。使学生更进一步明确结构决定性质,性质反映结构的辩证关系。
(3)及时进行归纳。乙炔是一个化学性质活泼的有机物,具有不饱和性,容易发生加成反应和氧化反应。乙炔的主要化学性质可以归纳如下:
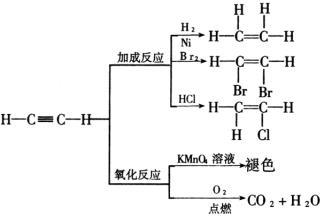
乙炔的一步加成产物的分子中含有一个碳碳双键,乙炔的线型结构变为平面型结构,由于乙炔的一步加成产物仍含有不饱和结构,还可继续跟![]() 发生加成反应,乙炔的加成能力一般是乙烯的二倍。
发生加成反应,乙炔的加成能力一般是乙烯的二倍。