 设为首页
设为首页
 加入收藏
加入收藏
教学设计方案(一)
实验准备
每组学生2人。课前备好的实验用品有氨水、硫铵、碳铵、尿素、硝铵、氯化铵、草木灰、氢氧化钠溶液、红色石蕊试纸、石灰、蒸馏水、试管、玻璃棒、酒精灯等。
教学过程
师:请举出含有氮元素的酸、碱、盐。
【练习】三位学生上黑板分别写出含氮元素的酸、碱、盐,其他同学做在笔记本上。(教师巡视。)
师:再请一名同学上黑板订正差错。
(学生在预习后能写出HNO3、NH3・H2O、NH4NO3、(NH4)2SO4、NH4HCO3、CO(NH2)2。如果学生写不出,可由教师写。)
师:请算出NH4HCO3、NH4NO3、(NH4)2SO4和CO(NH2)2的含氮百分率。
【练习】四位学生上黑板,教师巡视。
【引言】在酸、碱、盐各类化合物中,特别是盐类中,有好多种含有农作物所需要的营养元素,因而可以用作肥料。这种以矿物、空气、水为原料,经化学或机械加工制成的肥料叫做化学肥料,简称化肥。化肥分氮肥、磷肥、钾肥、微量元素肥料和复合肥料等。(给学生看实物:氮肥、磷肥、钾肥等。)
【板书】化肥
一、氮肥
师:目前农业上常用的氮肥有哪些?主要作用是什么?
生:氨水、碳铵和尿素,供作物的茎和叶生长。
师:碳铵是铵盐中的一种,还有硫铵(肥田粉)、硝酸铵等。
【板书】1.氨水――氨气的水溶液。2.铵盐。3.尿素(分别写在设计好的黑板的某位置上。)
【实验】请大家做实验:往氨水中滴加酚酞溶液后,再加热煮沸,观察发生的现象。
【实验】教师巡视,学生讨论,讲现象(往氨水中滴入酚酞溶液显红色,加热煮沸,红色消失)。
师:请同学归纳氨水的性质。
生:(1)无色液体,有刺激性气味,(2)显碱性,(3)易挥发。
(学生边回答,教师边板书。)
师:怎样保存氨水?
生:密封在容器里,放在阴凉处,也可在氨水的表面覆盖一层矿物油。(后一句学生答不出,可由老师讲。)
师:氨水是液体,运输不便,容易挥发而降低肥效,想什么办法使氨水便于贮存、运输。
生:生产上常用酸跟氨反应,生成固体铵盐用作肥料。
【演示】做硝酸、硫酸、盐酸分别跟氨反应的实验,现象有什么不同?
生:盐酸和硝酸遇氨冒白烟,硫酸跟氨反应不冒烟。
师:氨遇挥发性酸冒白烟。
【实验】硝铵、硫铵的水溶性和加热碳铵、氯化铵。
师:这两个实验说明铵盐有哪些性质?
【讨论】(1)大都是白色固体,易溶于水。(2)都易分解,一般生成氨和相应的酸。(学生边讨论,老师边板书。)
【练习】同学上黑板写化学方程式。

【演示】硫铵、氯化铵跟熟石灰共热,用湿润的红色石蕊试纸检验氨。引导学生看书回答铵盐在贮存和使用时应注意的问题。
生:看书、讨论,回答问题。
【板书】铵盐跟石灰、草木灰等碱性物质混合会放出氨,降低肥效(写在铵盐后面)。
(NH4)2SO4+Ca(OH)2 ![]() CaSO4+2H2O+2NH3↑
CaSO4+2H2O+2NH3↑
2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
在教师指导下由学生写化学方程式,并指出实验室可用固体氯化铵和熟石灰制取氨。
请同学们做实验:用氢氧化钠溶液、红色石蕊试纸等证明硫酸铵中存在NH4+
【实验】教师巡视指导。
师:写出该实验的化学方程式。
【练习】一学生上讲台写,其他学生在笔记本上练。
(NH4)2SO4+2NaOH
![]() Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O
师:引导学生看课本上讲的碳铵、硝铵、硫铵的特点,铵盐的含氮质量分数,硝铵使用时的注意事项和尿素的性质。
【板书】存在于动物尿中(写在尿素的后面)。
【讲解】尿素是白色粒状晶体,易溶于水,含氮量高达46%。尿素施入土壤受微生物作用后变成碳酸铵,易被作物吸收,工业上可用人工方法制取(拓宽知识面)。
师:农业上除了使用氮肥外,还有什么肥料?
生:磷肥、钾肥。
【板书】二、磷肥
三、钾肥(写在黑板上相应的位置)
师:磷肥的作用是什么?
生:促进作物根系发达,增强抗寒、抗旱能力,还能促进作物提早成熟,穗粒增多,籽粒饱满。
【板书】作用于根系和籽粒(写在磷肥后面)
师:农村用得比较多的磷肥是什么?
生:过磷酸钙
【板书】(2)过磷酸钙――磷酸二氢钙和硫酸钙的混合物(普钙),能溶于水。
![]()
(知识适当拓宽。)
师:磷肥还有哪些?请看书。
生:看书,回答问题。
【板书】(1)磷矿粉――Ca3(PO4)2,难溶于水(写在过磷酸钙上面)。
(3)重过磷酸钙――Ca(H2PO4)2,能溶于水,简称重钙。
Ca3(PO4)2+4H3PO4===3Ca(H2PO4)2
(知识适当拓宽。)
(4)钙镁磷肥
师:强调普钙、重钙都不宜与碱性物质接触,制过磷酸钙或重钙的目的是使不溶性的磷矿石转化为易溶于水的磷酸盐,易被作物吸收。(可在学生看书、讨论基础上得出。)
师:钾肥的作用是什么?
生:能促使作物生长健壮、茎杆粗硬,增强对病虫害和倒伏的抵抗能力,并能促进糖分和淀粉的生成。
【板书】作用于茎杆、块根、块茎(写在钾肥后面)。
师:引导学生看书,回答钾肥的性质及施用方法。目前农村常用的钾肥是什么?
(学生回答略。)
师:植物生长需要大量的氮、磷、钾营养元素,还需要微量元素。
【板书】四、微量元素肥料
师:请同学们找出微量元素。
生:铜、硼、锌、锰和钼。
师:在今天我们所学的内容中,找出含两种以上营养元素的化肥。
生:(NH4)3PO4、KNO3(答错可讨论、订正。)
【板书】五、复合肥料
师:除使用化肥外,我国农村大量使用的农家肥料还有哪些?
生:厩肥、绿肥、粪肥等。
师:请大家再看书,比较化肥、农家肥的特点,并小结本节课的重点。
(学生小结略。)
【练习】1.常用的含氮化肥有______,含磷化肥有______,含钾化肥有______。
2.在贮存、运输和施用氨水、碳酸氢铵、草木灰等肥料时应怎样防止肥分损失?
3.有四瓶溶液,分别是硫酸铵、石灰水、盐酸和稀硫酸,用什么化学方法来鉴别它们?
【作业】1.现有含氮15%的氨水40kg,要用水稀释到含氨0.3%才能施用,需要加水多少千克?
2.理论上生产400t硝酸铵,需要多少吨氨和多少吨溶质的质量分数为70%的硝酸?
3.有不纯的硫铵样品,经分析知道它含20%的氮,求样品里含硫酸铵的质量分数。
教学说明
本堂课采用边讲边实验、边练习的方法,把化肥的性质、作用及施用时的注意事项,直观而生动地介绍给学生。用意在于激发学生学习兴趣,培养学生动手能力、观察能力和思维能力,并注意开拓学生视野,适当拓宽知识面。整堂课力求体现顺应学生认知结构,实现知识和能力的同步到位。
专家评注
本堂课自始至终以学生为主体,采用边讲、边实验、边练习的方法,让学生了解化肥的性质、作用和施用时的注意事项。教师引用得法,学生学得主动。通过看书、归纳、对比,培养学生的自学能力,实现知识与能力的同时到位。
在教学中理论联系实际,使学生掌握的知识能学以致用,有利于激发学生学习化学的兴趣。
教学设计方案(二)
实验准备
氨水、碳酸氢铵、硝酸铵、硫酸铵、氯化铵、尿素、熟石灰、蒸馏水、磷矿石、过磷酸钙、草木灰。
试管、试管夹、试管架、玻片、玻棒、酒精灯、火柴、红色石蕊试纸、小黑板、植物生长图表、铁架台。
教学过程
【引言】肥是农家宝,庄稼少不了。农家常用的肥料有绿肥、河泥、发酵的粪尿,但量少、使用不方便,且缺乏营养素。人们用化学方法制得的化肥,在农业上已广泛使用。解放前全国只有两个化肥厂,现在中国的化肥除了自用外,还能部分出口。
【板书】化肥
【自问自答】常用的化肥有哪些?
有氮肥、磷肥、钾肥、复合肥料(如磷酸二氢钾)、微量元素肥料(如Cu、Fe)、钙素肥料(如硫酸钙)等,这节课主要讲氮肥、磷肥和钾肥。
【提问】植物为什么需要氮肥、磷肥和钾肥?
(看图表后小议)
【小结】氮元素可使植物细胞加速分裂和生长,促进植物枝叶茂盛。磷元素使植物提早开花结果,增强抵抗力。钾元素有利光合作用,促进作物生长健壮。这三种元素都是植物生长不可缺少的成分。
【问】哪些物质属于氮肥?它们有哪些重要的性质和特点?
【看实物】色、态、味

【板书】一、氮肥
【列表】

【分析】各种氮肥的优缺点。
氨水 它是氨的水溶液,浓度一般是20%左右。氨水是混合物,含有NH3、H2O、NH3・H2O、NH4+、OH-等微粒。它加工简单,使用方便,易分解,易挥发,使用时必须稀释。某学生在一次劳动时把氨水直接浇在作物上,没多久,茎叶顷刻变黄。
碳酸氢铵 它长期使用也不会影响土质,受热易分解,所以要防潮和防曝晒。
硫酸铵 硫酸铵性质较稳定,长期使用土壤易结块、硬化,要定期用熟石灰改良土壤(但熟石灰切勿和肥料同时使用)。
尿素 尿素含氮量高,肥效持久,溶液呈中性。1kg尿素相当于100kg人粪尿或10kg菜子饼的含氮量,但成本较高,肥效缓慢。
硝酸铵和氯化铵 这两种肥料主要用于工业生产(如炸药和焊接等)。
【实验】学生两人一组。
在玻片上放少量碳铵,再加一些消石灰,用玻棒搅拌后闻气味。
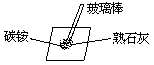
【结论】有刺激性气味的氨气逸出,这是快速检验铵盐的方法。例如,一农民为了检验某氨态化肥,先取极少量肥料放在手心,再加一点石灰,用手轻轻一搓,根据经验就可以得出结论。
【讲述】另一种化肥碳酸铵,分解产物是氨气、水、二氧化碳。它对土质无危害。上海郊区使用的氮肥中70%以上是碳铵。某化肥厂年产氨2万吨,制成的碳铵所增产的粮食可供100万人吃一年。
我国最早使用的氮肥是硫酸铵(硫铵),俗名肥田粉。尿素的含氮量高,所以发展较迅速。无论施用哪种铵态氮肥,都不能跟碱性物质同时使用,否则会放出氨气,降低肥效。
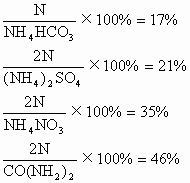
【练习】利用化学式求部分氮肥的含氮量。
【板书】二、磷肥
【自问自答】磷肥的主要成分是什么?它是含有磷酸根的盐。天然存在的磷酸盐是磷矿石(含磷酸钙),它不溶于水,怎么办?设法让它转化成可溶于水的磷酸盐。怎么转化?用硫酸跟磷矿石反应,生成能被植物吸收的磷酸二氢钙和硫酸钙(两者的混合物又叫过磷酸钙)。
![]()
【提问】
(1)把磷酸二氢钙施在碱性土壤中好吗?为什么?(它会转化成磷酸钙。)
(2)如果把磷矿石粉末施在酸性很强的土壤中,怎么样?(它会转化成磷酸二氢钙。)
【实物】展示磷矿石标本和过磷酸钙。
【板书】三、钾肥
【讲述】钾肥有碳酸钾、硫酸钾、氯化钾等,农村中常用的钾肥是草木灰(主要成分是碳酸钾,它的水溶液呈碱性)。不少地区,尤其是在平原地区,当人们把粮食脱粒以后,将作物的杆、茎就地烧成草木灰,既节省劳动力,又增加土中大量的钾肥。
【实物】草木灰
【提问】
(1)铵盐能不能跟草木灰同时使用,为什么?(会放出氨气,损失肥效。)
(2)磷酸二氢钙能不能跟草木灰同时使用,为什么?
(会生成难溶于水的磷酸钙。)
【小结】合理使用肥料非常重要,施肥应当因地制宜,考虑肥料的性质、土质、土层深浅、气候、时间、肥料的用量和地区的实际情况,把所学的知识结合起来。科技兴农,让化肥更有效地为人类造福。
【思考】(写在小黑板上)填空
l.氨水见光后易挥发和分解,所以容器口必须密封,且放在棕色瓶中。
2.硝铵在高温或猛烈撞击时会爆炸,碳铵在受热时会全部分解成气体。尿素的含氮量最高,肥效持久。铵盐跟碱性物质反应,会放出氨气。
3.磷酸二氢钙是溶于水的磷肥,它是用磷酸钙跟硫酸反应制成的。
4.草木灰中的钾肥主要成分是碳酸钾,它的水溶液呈碱性。
5.磷酸二氢钾是含钾、磷元素的复合肥料,硝酸钾是含钾、氮元素的复合肥料。
教学说明
通过实物、简单实验、运算、列表对比等手段,增强学生对化肥知识的识记能力。又通过实例和启发,克服教学内容的单调和枯燥,提高城镇学生对化肥的兴趣和重视程度。
专家讲评
“化肥”一节教材内容较多,执教者在处理教材上独具匠心,轻重缓急不同对待。
通过实物和图片,创设情景激发学生的学习兴趣;通过对氨水、碳铵和尿素等的对比,构建对氮肥认知上的关联;通过氮肥“跑氨”现象的分析,提高学生正确使用化肥的认识。
如果能在课前组织部分学生访问农家,或访问园艺工人,或开展课外小组活动,在课内由学生汇报化肥使用的状况,这对活跃课堂气氛,增强学生的社会责任感会有益处。